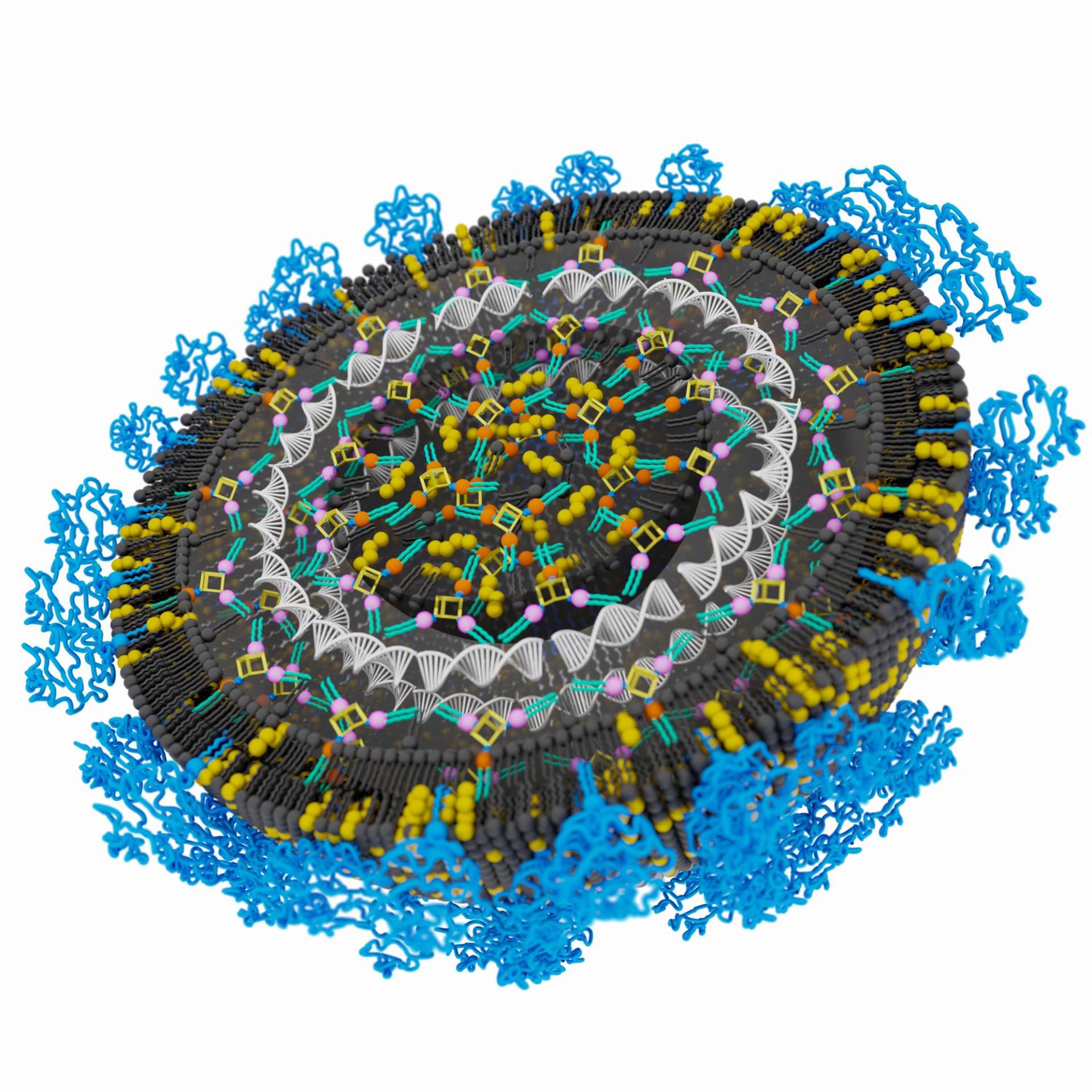
Systém pre dopravu nukleových kyselín do buniek svojím univerzálnym použitím prekonáva doterajšie riešenia a môže nájsť široké uplatnenie v liečbe genetických ochorení či v populárnych mRNA vakcínach.
Výsledky výskumu boli zverejnené v prestížnom časopise Advanced Functional Materials. Nové látky už boli patentované a získali si pozornosť partnerov z farmaceutického priemyslu.
Vedci z Ústavu organickej chémie a biochémie (ÚOCHB) českej Akadémie vied (AV ČR) objavili nový typ látok schopných bezpečne transportovať do buniek rôzne typy nukleových kyselín, ktoré sa používajú na liečebné účely, od základných stavebných kameňov až po dlhé reťazce RNA či DNA. Informoval o tom ústav na svojej stránke.
Ako spresnili českí výskumníci, nukleové kyseliny DNA a RNA sú známe predovšetkým ako nositelia genetickej informácie. Dnes je verejnosti známa hlavne molekula mRNA, ktorá je základom vakcín proti ochoreniu Covid-19.
Molekula mRNA plní funkciu pomyselného receptu pre syntézu konkrétneho proteínu, napríklad spike proteínu koronavírusu, proti ktorému si organizmus následne začne prirodzenou cestou vytvárať protilátky. K tejto syntéze dochádza vo vnútri bunky, kam sa preto najprv musí patričná molekula bezpečne dostať.
Unikátna zmes lipidov
„RNA je veľmi nestabilná látka, ktorá podlieha rýchlemu rozpadu. Aby sa vôbec mohla dostať do bunky, treba ju zabaliť do transportného obalu, ktorý ju ochráni pred okolitým prostredím a súčasne zaistí bezpečnú prepravu organizmom do bunky,” vysvetlila Klára Grantz Šašková zo skupiny Proteázy ľudských patogénov pri ÚOCHB.
V terapii sa k tomu využívajú lipidy skombinované s ďalšími molekulami, ktoré majú schopnosť zhlukovať sa s RNA a vytvárať tak nanočastice, v ktorých je nukleová kyselina ukrytá pred okolím. Tento princíp využívajú aj najnovšie mRNA vakcíny proti koronavírusu.
Lipidická častica XMAN pre ľahkú dopravu rôznych nukleových kyselín do bunky na terapeutické účely
„Vzhľadom na to, že pre každú cielenú terapiu sa používajú rôzne molekuly RNA odlišnej veľkosti, bolo až doteraz treba nájsť pre každý konkrétny druh RNA unikátnu zmes lipidov schopnú molekulu zabaliť, dopraviť a uvoľniť do bunky. Takýto nový obal navyše nesmie byť pre ľudské telo toxický, čo výrazne komplikuje a predlžuje vývoj,” spresnil Petr Cígler, vedúci skupiny Syntetickej nanochémie pri ÚOCHB.
Nový typ nanočastíc
Tím vedcov z Ústavu organickej chémie a biochémie AV ČR (ÚOCHB) vedený Petrom Cíglerom a Klárou Grantz Šaškovou, v spolupráci s vedcami z Ústavu molekulárnej genetiky AV ČR, Univerzity Karlovej a centra BIOCEV, teraz objavil nový typ nanočastíc, ktoré sú schopné bez ďalších zložitých úprav doručiť do buniek nukleovej kyseliny rôznej dĺžky, od základných stavebných kameňov nukleových kyselín cez krátke siRNA (používané v génových terapiách) až po mRNA či dlhé reťazce DNA.
Tieto nanočastice, nazvané XMAN, nie sú pre telo toxické a sú schopné ľahko preniknúť do bunky a uvoľniť svoj náklad s porovnateľnou účinnosťou pre väčšinu skúmaných nukleových kyselín.
Výhody XMAN
„Špecifikum našich látok je, že fungujú univerzálne. To znamená, že dopravujú do buniek akýkoľvek typ nukleových kyselín, a to s veľmi podobnou efektivitou. Sú pritom schopné bezpečne sa dostať aj do tak ťažko preniknuteľných buniek, ako sú napríklad ľudské primárne pečeňové bunky alebo bunkové línie z rôznych hematologických nádorov,” prezradila Klára Grantz Šašková.
Prierez časticou XMAN
Podľa Petra Cíglera je ďalšou veľkou výhodou ich dlhodobá stabilita pri relatívne bežných teplotách. „Oproti už používaným mRNA vakcínam, ktoré je nutné uchovávať pri mínus 70 stupňoch Celzia, môžu byť naše nanočastice skladované niekoľko mesiacov v obyčajnej chladničke,” doplnil.
Schopnosť doručovať do bunky molekuly rôznej veľkosti uľahčuje využitie systému aj vo veľmi odlišných génových terapiách. Okrem mRNA ide napríklad o choroby ako hemofília A či cystická fibróza spôsobené nedostatočnou tvorbou určitého proteínu. Molekula mRNA v takom prípade bunke umožňuje chýbajúci proteín vyrobiť.
Rovnako tak je ale možné využiť nových molekúl pri liečbe chorôb spôsobených naopak nesprávnu tvorbou patologických proteínov, napr. pri niektorých formách život ohrozujúcej amyloidózy, pri ktorej problémy spôsobuje proteín transthyretin.
V takom prípade je možné do bunky doručiť krátky úsek RNA označovaný siRNA ("malá interferujúca RNA"), ktorý je po vstupe do bunky schopný cielene tvorbu škodlivého či nesprávne fungujúceho proteínu vypnúť.
Ďalší výskum nových lipidových nanočastíc by mohol viesť k cielenej doprave do konkrétnych typov buniek, čo je žiaduce napríklad pre vývoj personalizovaných protinádorových vakcín alebo RNA liekov na liečbu neurodegeneratívnych ochorení.